Թեմա- Նյութի զանգվածի պահպանման օրենք
Լաբորատոր փորձ

Լաբորատոր փորձ

Թեմա՝ Քանակաչափություն։ Նյութի քանակ ։Մոլ։Մոլային զանգված
Քիմիական ռեակցիաների ընթացքում փոխարկվում են նյութի տվյալ չափաբաժնում պարունակվող կառուցվածքային մասնիկները (ատոմները, մոլեկուլները, իոնները): Ուստի նյութի զանգվածի և ծավալի հետ մեկտեղ անհրաժեշտ է իմանալ այդ մասնիկների թիվը: Այդ պատճառով քիմիայում օգտագործվում է նյութի քիմիական քանակ (նյութաքանակ) ֆիզիկաքիմիական մեծությունը` 𝑛 :

Նյութի քանակը տվյալ նյութի չափաբաժինն է, որը պարունակում է այդ նյութի որոշակի թվով կառուցվածքային միավորներ:
Նյութի քիմիական քանակի չափման միավորը մոլն է ( լատիներեն նշանակում է քանակ):
Մեկ մոլը նյութի այն քանակն է, որն այնքան կառուցվածքային միավոր (ատոմ, մոլեկուլ, կամ այլ մասնիկ) է պարունակում, որքան ատոմ է պարունակվում ածխածնի 𝐶12 իզոտոպի 0,012 կգ -ը:
Տվյալ նյութի քանակը իմաստավորվում է, եթե որոշակիորեն նշվում է նյութի տեսակը, այսինքն, թե ինչ կառուցվածքային մասնիկներից է այն կազմված: Օրինակ՝ «բրոմի մեկ մոլ» արտահայտությունը թերի է, քանի որ այն կարող է վերաբերվել և’ մեկ մոլ 𝐵𝑟2-ին, և’ մեկ մոլ 𝐵𝑟-ին, իսկ մոլեկուլային բրոմը և ատոմային բրոմը տարբեր կառուցվածքային մասնիկներ են:
Նյութի քանակ արտահայտության մեջ նյութբառն օգտագործվում է ընդարձակ մատերիա իմաստով: Այդ պատճառով կառուցվածքային մասնիկների թվին են դասվում պրոտոնները, էլեկտրոնները և ֆիզիկական մյուս մասնիկները, որոնք ինքնըստինքյան քիմիական նյութեր չեն առաջացնում:
Վարժություններ
1)Որքան է մոլեկուլների թիվն ածխածնի (IV) օքսիդի (CO2) 22 գ զանգվածով նմուշում:
2)Որքա՞ն է ատոմների թիվը էթանի (C2H6 ) 15 գ զանգվածով նմուշում:
1) քիմիական հավասարում
3) քիմիական ռեակցիա
4) քիմիական տարր
2) քիմիական բանաձև
2)Ո՞ր մասնիկներն են ատոմի միջուկում, որը(որոնք)՝ էլեկտրոնային
1) պրոտոն, էլեկտրոն և նեյտրոն
2)պրոտոն և էլեկտրոն, նեյտրոն
3) նեյտրոն և պրոտոն, էլեկտրոն
4) նեյտրոն և էլեկտրոն, պրոտոն
թյունները պարբերություններում ձախից աջ.
1) մետաղականն ուժեղանում է, ոչ մետաղականը՝ թուլանում
2) մետաղականը թուլանում է, ոչ մետաղականը՝ ուժեղանում
3) մետաղականը մնում է անփոփոխ, ոչ մետաղականը՝ թուլանում
4) մետաղականը թուլանում է, ոչ մետաղականը՝ մնում անփոփոխ
1) իոնային
2) կովալենտային բևեռային
3) կովալենտային ոչ բևեռային
4) իոնային և կովալենտային ոչ բևեռային
1) ազոտ
2) նեոն
3) քլոր
4) ջրածին
1) օդից թեթև է
2) ջրում համարյա անլուծելի է
3) անհոտ է և անգույն
4) այրվում կամ պայթում է օդում
Թեստ 2
1) օդ
2) շաքարաջուր
3) կաթ
4) կերակրի աղ
1) գույնի
2) միմյանց մեջ չլուծվելու
3) մագնիսական հատկությունների
4) մոլեկուլների չափերի
1) միայն ֆիզիկական
3) նախ ֆիզիկական, ապա քիմիական
2) միայն քիմիական
4) նախ քիմիական, ապա ֆիզիկական
4)Հետևյալներից ո՞րն է հիմնային օքսիդի բանաձև.
1) Li2Օ
2) C02
3) S03
4) Si02
5)Ո՞ր բյուրեղավանդակն է համապատասխանում կերակրի աղին.

6)Համապատասխանեցրե՛ք տարրի նշանը և այդ տարրի ատոմի հիմնական վիճակի էլեկտրոնային բանաձևը.

Պատասխանել հարցերին՝
1)Հետևյալ տարրերից որի՞ ատոմի արտաքին էներգիական մակարդակն է պարունակում այնքան էլեկտրոն, ինչքան ազոտի ատոմինը.
1) ածխածին
2) թթվածին
3) ֆոսֆոր
4) ֆտոր
Քանի որ արտաքին էներգիական մակարդակում միևնույն թվով Էլեկտրոններ պարունակում են նույն ենթախմբի տարրերի ատոմները, ապա հարցին ճիշտ պատասխանելու համար պետք է գտնել այն տարրը, որն ազոտի հետ միասին գտնվում է միևնույն ենթախմբում:
2)Ո՞ր շարքում են տարրերը դասավորված ըստ ոչ մետաղական հարկությունների ուժեղացման,
1) Si, P, S
2) O, C, F
3) Cl, S, P 4) F, Cl, Br
Այս առաջադրանքը պահանջում է հատկությունների համեմատում: Քանի որ պարբերություններում միջուկի լիցքի մեծացման հետ ձախից աջ ոչ մետաղական հատկություններն ուժեղանում են, հետևաբար՝ ճիշտ պատասխանը Si, P, S դասավորությունն է:
3)Ո՞ր տարրի բարձրագույն օքսիդին համապատասխան թթուն առավել ուժեղ,
1) S
2) Si
3) Cl
4) P
Դիտարկելով` առաջադրանքում տրված տարրերի դիրքը պարբերական համակարգում՝ տեսնում ենք, որ բոլորը երրորդ պարբերու– թյան տարրեր են: Գիտելիքները նույն պարբերության օքսիդների և հիդրօքսիդների թթվահիմնային հատկությունների փոփոխության օրինաչափությունների վերաբերյալ հնարավորություն են տալիս ընտրելու ճիշտ պատասխանը:
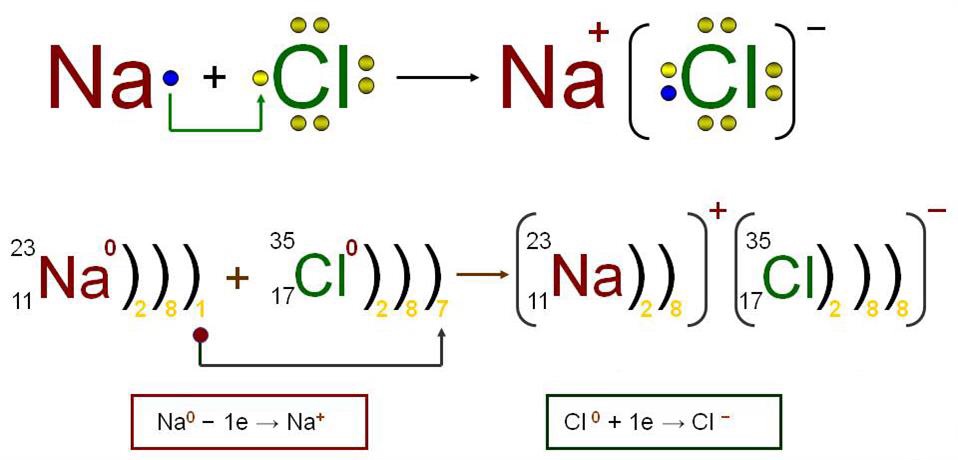
Քիմիական կապի տեսակները: Իոնային կապ
Քիմիական կապը ատոմների միջև փոխազդեցություն է, ինչի արդյունքում առաջանում են մոլեկուլներ (բյուրեղներ):
Ատոմներից մոլեկուլների առաջացման «շարժիչ ուժը» ատոմի արտաքին էլեկտրոնային շերտի ութ (երբեմն երկու) էլեկտրոն պարունակող կայուն (ավարտուն) վիճակն է, որին ձգտում են ատոմները: Հենց դա է իներտ գազերի՝ բնության մեջ առանձին ատոմների ձևով գտնվելու պատճառը:


Քիմիական կապն ունի էլեկտրական բնույթ: Այն իրականանում է քիմիական կապին մասնակցող ատոմների միջուկների և էլեկտրոնների էլեկտրաստատիկական փոխազդեցության (և՛ ձգողության, և՛ վանողության) շնորհիվ:

Քիմիական կապի առաջացմանը մասնակցում են ատոմի վալենտային էլեկտրոնները:
Ատոմներից մոլեկուլների առաջացումն ուղեկցվում է ջերմության անջատմամբ, հետևաբար՝ մոլեկուլներն ավելի կայուն համակարգեր են, քան նույն մոլեկուլներն առաջացնող ատոմները:
Քիմիական կապի էներգիան տատանվում է լայն տիրույթում (40-ից մինչև 1000 կՋ/մոլ), ինչը պայմանավորված է ատոմների միջև տարբեր տեսակի փոխազդեցություններով:
Ներկայումս տարբերում են քիմիական կապի մի քանի տեսակներ՝ իոնային, կովալենտային, մետաղական և ջրածնային: